Pengetesan dalam jumlah besar dan akurat merupakan salah satu kunci penanganan pandemi COVID-19. Hingga saat ini tes PCR adalah standar emas pemeriksaan COVID-19. Namun para ilmuwan juga mengembangkan tes uji molekuler khusus untuk virus SARS-CoV-2 ini, yang hasilnya lebih cepat (dibanding tes PCR) dengan akurasi lebih baik (dibanding rapid test antigen).
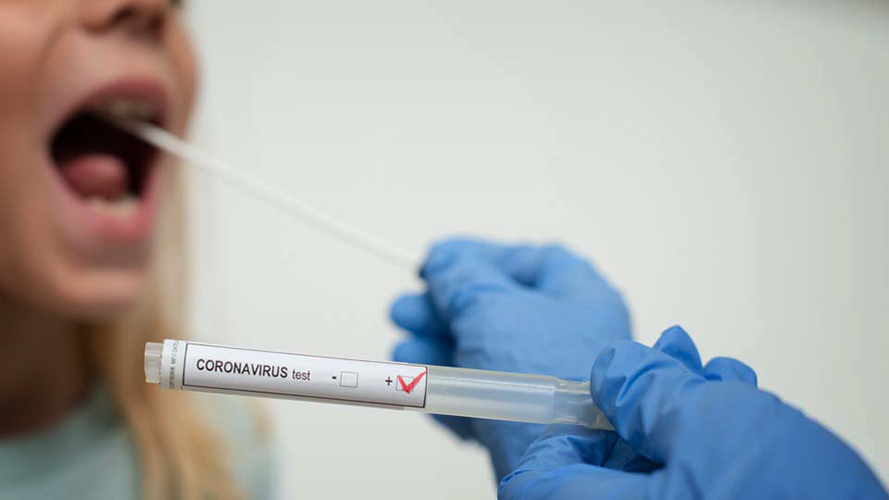
Tes PCR (Polymerase Chain Reaction) menggunakan sampel lendir dari hidung atau tenggorokan untuk mendeteksi keberadaan virus. Tes ini untuk mendeteksi materi genetik (DNA dan RNA) dari suatu sel, kuman atau virus, termasuk virus corona.
Tingkat akurasinya cukup tinggi, hanya saja metode pemeriksaan ini membutuhkan waktu sekitar 1-7 hari untuk mendapatkan hasilnya karena melalui dua kali proses yaitu, ekstraksi dan amplifikasi.
Metode lain yang dikembangkan para ilmuwan adalah tes uji molekuler / tes cepat molekuler (TCM). Tes ini sejatinya adalah tes PCR yang disederhanakan. Pemeriksaan dengan TCM sama akuratnya dengan PCR karena bisa mengidentifikasi RNA dari SARS-CoV-2, tetapi dalam waktu relatif lebih singkat.
Tes ini sudah digunakan untuk penyakit tuberkulosis (TB). Metode pemeriksaannya menggunakan dahak – seperti tes PCR - dengan amplifikasi asam nukleat berbasis cartridge.
Virus SARS-CoV-2 diidentifikasi pada RNA-nya menggunakan cartridge khusus. Hasil tes bisa diketahui dalam waktu kurang lebih dua jam. Pemerintah telah melakukan pemeriksaan menggunakan TCM ini di 132 rumah sakit dan puskesmas yang ditunjuk.
AccuraDtect
Salah satu alat tes molekuler yang akan datang di Indonesia adalah AccuraDtect; alat ini juga dipakai untuk penanganan pandemi di Korea. Awalnya alat ini dibuat oleh Genomictree, perusahaan layanan kesehatan yang mengembangkan diagnosis molekuler non-invasif untuk deteksi dini kanker.
Alat uji molekuler ini menyasar tiga biomarker untuk mengidentifikasi keberadaan virus corona yaitu RdRp, E dan N2. Hasilnya akan diperoleh dalam waktu empat jam setelah pengambilan sampel.
AccuraDtect rencananya akan segera dipakai di Indonesia setelah memperoleh izin edar. “Dengan diperolehnya izin edar ini, kami berharap bahwa penyediaan alat uji diagnostik unggulan Korea ini dapat berkontribusi besar dalam membantu upaya Indonesia mengatasi pandemi COVID-19,” kata Sengho Jeon, CEO dari DPCI (Daewoong Pharmaceutical Company Indonesia), dalam keterangan pers yang diterima OTC Digest, Jumat (23/10/2020).
Alat uji ini telah memperoleh sertifikasi CE-IVD (Perangkat Medis Diagnostik In Vitro bertanda CE) di Eropa pada bulan Maret lalu dan izin untuk penggunaan darurat (EUA) di Peru dan Singapura. (jie)