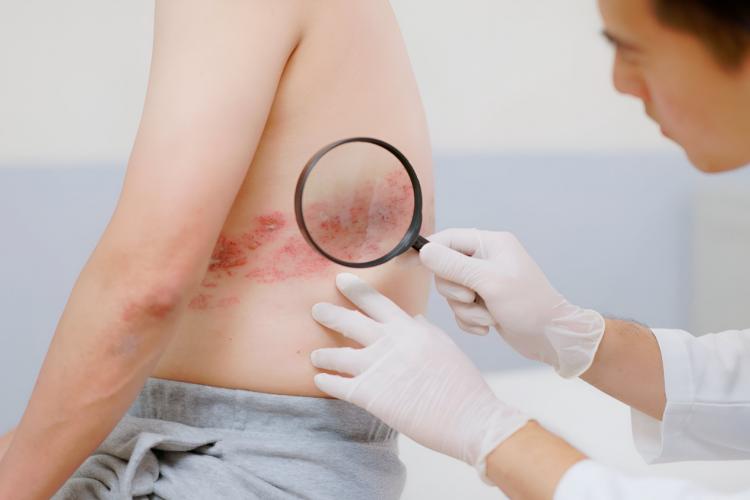
Menteri Kesehatan Terawan Agus Putranto mengatakan hingga saat ini belum pasti kapan vaksin COVID-19, yang awalnya akan didistribusikan November, bisa benar-benar tersedia di Indonesia. Faktor keamanan vaksin atas dasar uji klinis menjadi prioritas.
Dalam rapat paripurna bersama Komisi IX DPR RI, Selasa (17/11/2020), Menkes menjelaskan hingga saat ini pemerintah masih menunggu kedatangan vaksin setelah seluruh tahapan uji klinis selesai.
“Kalau ada kami informasikan dan pemimpin negara pasti akan memberitahukan. Kami memang dalam posisi wait and see kapan datangnya (vaksin),” ujar Terawan kepada DPR.
Terawan juga menambahkan, BPOM masih terus melakukan pemantauan terhadap produk vaksin COVID-19 yang bekerja sama dengan Bio Farma. Sebagaimana diketahui Bio Farma bekerja sama melakukan uji klinis fase 3 vaksin COVID-19 yang dikembangkan oleh Sinovac.
Pemerintah juga telah memesan vaksin lain dari Sinopharm/G42 dan Cansino, keduanya juga merupakan perusahaan dari China.
Vaksin COVID-19, imbuh Terawan, diharapkan tersedia secepatnya pada akhir tahun ini. “Namun, soal keamanan vaksin tetap menjadi prioritas,” katanya. “Green light (izin) bendera itu Badan POM sebagai otoritas yang punya wewenang untuk itu.”
Tidak bisa menggunakan data uji klinis di Brasil
Sebelumnya WHO telah memberikan wewenang bagi otoritas kesehatan negara setempat untuk mengeluarkan izin penggunaan darurat (Emergency Use Authorization / EUA), namun dengan persyaratan tertentu yang harus dipenuhi.
“Bisa memberikan EUA untuk vaksin COVID-19 diharuskan ada data uji klinik fase 1 dan 2 full report data 6 bulan, ditambah fase 3 interim analisis, jadi data 3 bulan,” terang Penny Lukito, Kepala BPOM, kepada Komisi IX DPR RI.
Sebelumnya dalam rencana penerbitan EUA, Indonesia akan menggunakan data uji klinis fase 3 vaksin Sinovac yang dilakukan di Brasil. Ini disebabkan data uji klinis fase 3 di Bandung belum memenuhi ketentuan tersebut.
Sinovac melakukan uji klinis fase 3 di empat negara, termasuk Indonesia, Chile, Turki dan Brasil dengan melibatkan lebih dari 20.000 partisipan. Tujuan uji klinis multicenter ini adalah untuk melihat efektivitas dan keamanan vaksin pada berbagai ras di dunia.
Namun, Brasil belum bisa memberikan data hasil uji klinis tersebut. Dilansir dari Kontan, Penny mengatakan, Indonesia akan menggunakan hasil uji klinis (data analisa interim 3 bulan) di Bandung yang diperkirakan baru dapat dikeluarkan EUA pada minggu ketiga Januari 2021.
Uji klinis fase 3 di Bandung saat ini telah masuk dalam tahap monitoring untuk melihat efikasi (khasiat), immunogenicity, serta memastikan keamanan calon vaksin COVID-19 tersebut.
Meski begitu, terdapat skema lain yang bisa mendorong penggunaan vaksin Sinovac pada Desember 2020 mendatang, yakni menggunakan skema compassionate use.
"Penggunaan bisa dilakukan dengan adanya permintaan dari kementerian," terang Penny.
Ia menjelaskan skema tersebut tetap akan menjamin mutu dan keamanan dari vaksin. Karena penggunaan skema tersebut juga mamakai data uji klinis fase 1 dan 2. Hanya saja belum terdapat data mengenai efikasi/efektivitas vaksin.
Penggunaan izin vaksin serupa juga telah dilakukan secara terbatas di China dan Uni Emirat Arab (UEA). Selain itu juga pernah dilakukan saat penggunaan vaksin ebola dan yellow fever sambil menunggu EUA. (jie)